
هر روز آن را در تبلیغات می بینید: کرم ها و لوسیون ها برای کاهش چین و چروک، رنگ هایی برای از بین بردن موهای خاکستری، و داروهایی برای کاهش درد عضلات و مفاصل. همراه با این تغییرات سطحی، افزایش سن بر فیزیولوژی داخلی بدن نیز تأثیر می گذارد، از جمله افزایش التهاب در مغز (Czirr & Wyss-Coray, 2012)، انحطاط در شبکیه چشم (هو کم و همکاران، 2010)، و نفوذپذیری دیواره های روده (Ma et al, 1992). بسیاری از صنایع با هدف معکوس کردن علائم پیری ساخته شده اند. اما آیا راهی برای مقابله با اثرات پیری در بدن در سطحی عمیق تر از رنگ کردن مو وجود دارد؟ یک گروه از دانشمندان راه منحصر به فردی را برای برگرداندن ساعت به عواقب مربوط به پیری در مغز با استفاده از انتقال میکروبیوتای مدفوع پیشنهاد می کنند (FMT؛ پارکر و همکاران، 2022).
FMT از اصول پارابیوزیس استفاده می کند (به مقاله واقعی Knowing Neurons مراجعه کنید اینجا کلیک نمایید!) برای مبادله میکروبیوم های روده، که به عنوان کل باکتری ها و میکروارگانیسم های زندگی در روده سالم تعریف می شود (سومر و همکاران، 2013)، بین موش های مسن و جوان. پارکر و همکارانش برای آزمایش فرضیه خود مبنی بر اینکه استفاده از FMT برای تغییر میکروبیوم روده باعث تغییر التهاب در مغز و بدن میشود، از یک مدل موش با موشهای 3 ماهه (موشهای جوان) و موشهای 24 ماهه (موشهای مسن) استفاده کردند. ). قبل از شروع آزمایش، محققان ابتدا مواد مدفوع را جمعآوری کردند تا پایهای را برای میکروبیومهای جوان و مسن موش تعیین کنند. پس از آن، به موش ها به مدت سه روز آنتی بیوتیک داده شد تا باکتری موجود در روده آنها کاهش یابد. پس از درمان آنتی بیوتیکی، محققان نمونه مدفوع دیگری را جمع آوری کردند. در ادامه این مراحل اولیه، دو نوبت FMT انجام شد که در آن مدفوع مایع از طریق بینی داده شد و موشها مطابق با گروه آزمایش خود در قفسهای حاوی مدفوع قرار گرفتند. گروههای آزمایشی در این مطالعه، موشهای مسن دریافتکننده FMT از موشهای جوان و موشهای جوان دریافتکننده FMT از موشهای مسن بودند، در حالی که گروههای کنترل، موشهای جوان دریافتکننده FMT از موشهای جوان دیگر یا محلول کنترل غیر مدفوعی (موسوم به موشهای کنترل جوان) بودند. موش های پیر دریافت کننده FMT از موش های مسن دیگر یا محلول کنترل غیر مدفوعی (موسوم به موش های کنترل پیر). پس از FMT، مدفوع پنج روز و دو هفته بعد جمع آوری شد. این طرح آزمایشی محققان را قادر ساخت تا بررسی کنند که چگونه سن میکروبیوم روده بر فرآیندهای مغز، شبکیه چشم و روده تأثیر می گذارد.
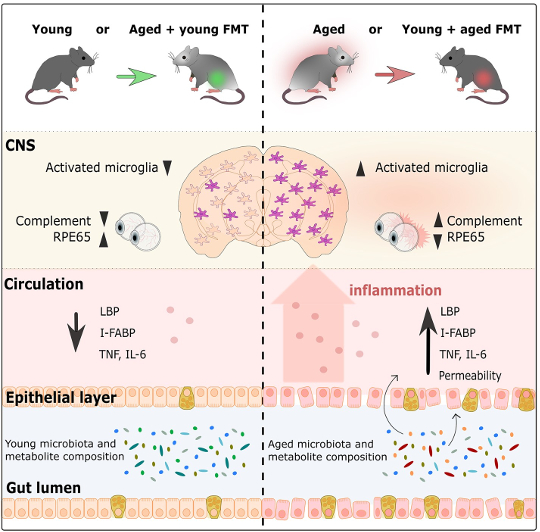
چکیده گرافیکی از پارکر و همکاران، 2022
... تزریق یک میکروبیوم جوان به موش مسن، پاسخ ایمنی را که با افزایش سن مشاهده می شود خنثی می کند.
محققان ابتدا بررسی کردند که چگونه FMT بر پاسخ التهابی میکروگلیا، سلولهای ایمنی ساکن مغز، در قشر و جسم پینهای (بسته عظیمی از نورونها که به دو طرف مغز اجازه میدهد با یکدیگر ارتباط برقرار کنند) تأثیر میگذارد (هنکا و همکاران، 2019). ارنی و همکاران، 2015). موشهای کنترل مسن نسبت به موشهای کنترل جوان میکروگلیا فعالتری داشتند که نشاندهنده روند پیری طبیعی است. با این حال، موشهای مسن با میکروبیومهای جوان نسبت به موشهای کنترل مسن، فعالسازی میکروگلیا بسیار کمتری داشتند. با کمال تعجب، پاسخ میکروگلیا کاملاً مشابه آنچه در موش های کنترل جوان مشاهده شد بود. این الگوی مشابه در جهت مخالف نیز نشان داده شد، زیرا موشهای جوان با میکروبیومهای مسن، نسبت به موشهای کنترل جوان، فعالیت میکروگلیا بسیار بیشتری داشتند، در عوض مشابه سطوح فعالسازی مشاهده شده در موشهای کنترل مسن. این نشان میدهد که سن میکروبیوم بر پاسخ ایمنی در مغز تأثیر میگذارد و تزریق میکروبیوم جوان به موش سالخورده، پاسخ ایمنی را که با افزایش سن مشاهده میشود خنثی میکند. به طور مشابه، دادن یک میکروبیوم مسن به موش جوان، تأثیر سن بر سلول های ایمنی مغز را تسریع می کند.
… میکروبیوم بر فرآیندهای مرتبط با افزایش سن در شبکیه تأثیر می گذارد…
علاوه بر بررسی مغز، محققان همچنین چگونگی تاثیر سن میکروبیوم روده بر شبکیه را بررسی کردند. به طور کلی، نشان داده شد که در مقایسه با موشهای جوان، موشهای مسن التهاب شبکیه را افزایش دادند. با این حال، پس از FMT، موشهای مسن با میکروبیومهای جوان سطوح التهاب شبکیه مشابه با موشهای کنترل جوان داشتند. مطابق با یافته های مغز، برعکس نیز صادق بود. موشهای جوان با میکروبیومهای مسن دارای التهاب شبکیه بودند که شبیه موشهای کنترل مسن بود. میکروبیوم روده همچنین بر بخش دیگری از سیستم بینایی تأثیر می گذارد: توانایی گیرنده های نوری برای بازسازی در شبکیه با کمک پروتئین RPE65 که تولید آن نیز با افزایش سن کاهش می یابد (Cai et al, 2009). در موشهای مسن با میکروبیومهای جوان، مقدار پروتئین RPE65 در مقایسه با موشهای کنترل مسن افزایش یافت. در واقع، این سطوح پروتئین مشابه سطوح در موش های جوان بود. علاوه بر این، موشهای جوان با میکروبیومهای مسن RPE65 بسیار کمتری نسبت به موشهای کنترل جوان داشتند، با سطوح پروتئین قابل مقایسه با سطوح مشاهده شده در موشهای مسن. به طور کلی، این نشان میدهد که میکروبیوم بر فرآیندهای مرتبط با افزایش سن در شبکیه تأثیر میگذارد، به طوری که میکروبیومهای جوان معکوس میشوند و میکروبیومهای مسن فرآیندهای مرتبط با پیری را تسریع میکنند.
اندام مهم دیگر، روده ها نیز از اثرات پیری در امان نیستند: لایه سلولی که دیواره روده را تشکیل می دهد به مرور زمان نشتی می یابد (Cui et al, 2019; Thevaranjan et al, 2017). در طول پیری، پایداری دیواره روده کاهش مییابد و نفوذپذیرتر میشود، که به باکتریها اجازه میدهد به محیط اطراف نشت کنند، که به نوبه خود التهاب کلی را افزایش میدهد (Cui et al, 2019; Thevaranjan et al, 2017). در این مطالعه، محققان نشان دادند که سن میکروبیوم بر پایداری دیوارههای روده تأثیر میگذارد. در موشهای مسن با میکروبیوم جوان، رودهها نسبت به موشهای کنترل مسن نشتی کمتری داشتند. در واقع، نفوذپذیری روده در موش های مسن با میکروبیوم جوان مشابه نفوذپذیری مشاهده شده در موش های جوان بود. موشهای مسن با میکروبیومهای جوان نیز سطوحی از التهاب و شواهدی از وجود باکتری در خون مشابه موشهای جوان داشتند. بار دیگر، رودههای موشهای جوان با میکروبیومهای مسن مانند موشهای مسن با میکروبیومهای مسن با داشتن روده نشتیتر و التهاب بیشتر نسبت به موشهای جوان با میکروبیومهای جوان رفتار کردند. این نتایج از این فرضیه حمایت میکند که میکروبیومهای پیر به افزایش نفوذپذیری روده کمک میکنند، که با اجازه دادن به باکتریها برای نشت به جریان خون، افزایش التهاب را تسهیل میکند. نکته مهم، معرفی یک میکروبیوم جوان از طریق FMT این اثرات مرتبط با سن را معکوس می کند.
... سن میکروبیوم روده بر عملکرد مغز، شبکیه چشم و روده تأثیر می گذارد.
نتایج این مطالعه نشان می دهد که سن میکروبیوم روده بر عملکرد مغز، شبکیه چشم و روده تأثیر می گذارد. اما میکروبیوم های جوان و پیر چه تفاوتی با یکدیگر دارند؟ برای پاسخ به این سوال، محققان DNA میکروبیوم یافت شده در نمونه های مدفوع جمع آوری شده در طول آزمایش را توالی یابی کردند. میکروبیوم جوان و مسن قبلاً قبل از وقوع FMT ساختارهای ژنتیکی متفاوتی داشتند، اما FMT به طور قابل توجهی ترکیب ژنتیکی هر دو میکروبیوم را تغییر داد. موشهای جوان با میکروبیومهای مسن، ترکیبی بسیار شبیه به موشهای کنترل مسن داشتند، در حالی که ترکیب ژنتیکی در موشهای مسن با میکروبیومهای جوان با موشهای کنترل مسن متفاوت بود و همچنین با موشهای جوان با میکروبیومهای جوان متفاوت بود - آنها در این بین بودند. موشهای کنترل مسن و موشهای جوان با میکروبیومهای مسن دارای باکتریهایی بودند که عمدتاً از این باکتریها بودند اسیلوباکتر و پرووتوتلا جنس ، Firmicutes شاخه، و لاکتوباسیلوس جانسونی گونهها، در حالی که موشهای کنترل جوان و موشهای مسن با میکروبیومهای جوان دارای باکتریهایی بودند که عمدتاً از این باکتری بودند بیفیدوباکتریوم, آکرمانزیا, پاراباکتروئیدها, کلستریدیومو انتروکوک گروه ها. هنگام بررسی علت بالقوه این تغییرات مرتبط با افزایش سن، محققان دریافتند که مسیرهای درگیر در تولید لیپید و ویتامین (که به متابولیت های تولید شده توسط باکتری ها متکی هستند) بین میکروبیوم های پیر و جوان متفاوت است. این مشاهدات یک اشکال دارد - تغییرات در فراوانی انواع مختلف باکتری ها و عملکرد بالقوه آنها در روده طولانی نبود، زیرا دو هفته پس از FMT تفاوت زیادی بین ترکیب میکروبیوم وجود نداشت.
به طور کلی، این مطالعه نشان داد که میکروبیوم روده بر فرآیندهای مرتبط با افزایش سن در مغز، چشم و روده تأثیر می گذارد. میکروبیومهای مسن، مستقل از سن موش گیرنده، منجر به التهاب بیشتر در مغز، شبکیه و رودهها، پتانسیل بازسازی کمتر در گیرندههای نوری در شبکیه، و نشت باکتریهای بیشتری از رودهها شد. از سوی دیگر، معرفی میکروبیومهای جوان به موشهای مسن این اثرات پیری را معکوس کرد. این ممکن است به دلیل تفاوت در ترکیب باکتریایی میکروبیومهای پیر و جوان، و تأثیری که این تغییرات ممکن است بر مسیرهای مسئول تولید لیپید و ویتامین داشته باشد. یک سوال که در این مطالعه به آن پرداخته نشد این بود که چگونه سن میکروبیوم بر عملکرد شناختی تأثیر می گذارد، زیرا نه موش های کنترل و نه موش های FMT در تست های حافظه رفتاری رفتار متفاوتی نداشتند. تحقیقات آتی نیز باید بر روی این سوال متمرکز شود زیرا شناخت و حافظه با افزایش سن کاهش مییابد و درک نقش میکروبیوم در زوال شناختی مرتبط با سن میتواند بینش مهمی را در زمینه زیربنای بیولوژیکی احتمالی ارائه دهد. جهت دیگری که سؤالات تحقیقاتی آینده باید دنبال شود تأثیر رژیم غذایی بر ترکیب میکروبیوم روده است. مطالعات قبلی نشان دادهاند که رژیمهای غذایی مختلف انواع میکروبهای روده را هم در کوتاهمدت (دیوید و همکاران، 2014) و هم در بلندمدت تغییر میدهند (وو و همکاران، 2011). اگر تغییر در رژیم غذایی می تواند ترکیب میکروبیوم روده را تغییر دهد، چه می شود اگر بتواند این علائم پیری را در مغز، شبکیه چشم و روده ها نیز کاهش دهد؟
اگر تغییر در رژیم غذایی می تواند ترکیب میکروبیوم روده را تغییر دهد، چه می شود اگر بتواند این علائم پیری را در مغز، شبکیه چشم و روده ها نیز کاهش دهد؟
درباره نویسنده
نوشته شده توسط هالی کورتاس، به تصویر کشیده شده توسط فدریکا راگوزو، ویرایش شده توسط یوهانا پاپ, سارا ویدو لورن واگنر
منابع
Cai، X.، Conley، SM، و Naash، MI (2009). RPE65: نقش در چرخه بینایی، بیماری شبکیه انسان و ژن درمانی. ژنتیک چشمی, 30(2)، 57-62. https://doi.org/10.1080/13816810802626399
Cui, H., Tang, D., Garside, GB, Zeng, T., Wang, Y., Tao, Z., Zhang, L., & Tao, S. (2019). سیگنال دهی Wnt باعث ایجاد اختلال در تمایز ناشی از پیری سلول های بنیادی روده می شود. بررسی ها و گزارش های سلول های بنیادی, 15(3)، 448-455. https://doi.org/10.1007/s12015-019-09880-9
Czirr، E.، و Wyss-Coray، T. (2012). ایمونولوژی تخریب عصبی مجله تحقیقات بالینی, 122(4)، 1156-1163. https://doi.org/10.1172/JCI58656
دیوید، ال.، موریس، سی، کارمودی، آر. و همکاران رژیم غذایی به سرعت و به طور قابل تکرار میکروبیوم روده انسان را تغییر می دهد. طبیعت 505، 559-563 (2014). https://doi-org.proxy.library.georgetown.edu/10.1038/nature12820
ارنی، دی، هراب؟ de Angelis، AL، Jaitin، D.، Wieghofer، P.، Staszewski، O.، David، E.، Keren-Shaul، H.، Mahlakoiv، T.، Jakobshagen، K.، Buch، T.، Schwierzeck، V. ., Utermöhlen, O., Chun, E., Garrett, WS, McCoy, KD, Diefenbach, A., Staeheli, P., Stecher, B., Amit, I., & Prinz, M. (2015). میکروبیوتای میزبان به طور مداوم بلوغ و عملکرد میکروگلیا را در CNS کنترل می کند. طبیعت اعصاب, 18(7)، 965-977. https://doi.org/10.1038/nn.4030
Heneka MT (2019). میکروگلیا در مرکز بیماری های نورودژنراتیو قرار دارد. بررسی طبیعت. ایمونولوژی, 19(2)، 79-80. https://doi.org/10.1038/s41577-018-0112-5
Hoh Kam, J., Lenassi, E., & Jeffery, G. (2010). مشاهده چشمهای پیر: مکانهای مختلف تجمع آمیلوئید بتا در شبکیه پیر موش و تنظیم بالای ماکروفاژها. PloS One, 5(10)، e13127. https://doi.org/10.1371/journal.pone.0013127
Ma, TY, Hollander, D., Dadufalza, V., & Krugliak, P. (1992). تأثیر افزایش سن و محدودیت کالری بر نفوذپذیری روده. جئونتولوژی تجربی, 27(3)، 321-333. https://doi.org/10.1016/0531-5565(92)90059-9
پارکر، آ.، رومانو، اس.، آنسورژ، آر.، ابوالنور، آ.، لو گال، جی، ساوا، جنرال موتورز، پونتیفکس، ام جی، تلاتین، آ.، بیکر، دی، جونز، ای.، واوزور , D., Rudder, S., Blackshaw, LA, Jeffery, G., & Carding, SR (2022). انتقال میکروبیوتای مدفوع بین موشهای جوان و مسن، علائم پیری روده، چشم و مغز را معکوس میکند. میکروبیوم, 10(1)، 68.
https://doi.org/10.1186/s40168-022-01243-w
سامر، اف.، و باکهد، اف. (2013). میکروبیوتای روده - استادان رشد و فیزیولوژی میزبان بررسی های طبیعت. میکروبیولوژی, 11(4)، 227-238. https://doi.org/10.1038/nrmicro2974
Thevaranjan، N.، Puchta، A.، Schulz، C.، Naidoo، A.، Szamosi، JC، Verschoor، CP، Loukov، D.، Schenck، LP، هیئت داوران، J.، Foley، KP، Schertzer، JD، Larché، MJ، Davidson، DJ، Verdú، EF، Surette، MG، و Bowdish، DME (2017). دیسبیوز میکروبی مرتبط با سن باعث افزایش نفوذپذیری روده، التهاب سیستمیک و اختلال عملکرد ماکروفاژها می شود. میزبان سلولی و میکروب, 21(4) ، 455–466.e4. https://doi.org/10.1016/j.chom.2017.03.002
وو، جی دی، چن، جی.، هافمن، سی، بیتینگر، کی، چن، یی، کیلباگ، SA، بیوترا، ام.، شوالیه، دی.، والترز، WA، نایت، آر.، سینها، آر. ، گیلروی، ای.، گوپتا، ک.، بالداسانو، آر.، نسل، ال.، لی، اچ.، بوشمن، FD، و لوئیس، JD (2011). ارتباط الگوهای غذایی طولانی مدت با انتروتیپ های میکروبی روده علوم (نیویورک، نیویورک), 334(6052)، 105-108. https://doi-org.proxy.library.georgetown.edu/10.1126/science.1208344
این مقاله در ابتدا در ظاهر دانستن نورون ها






















